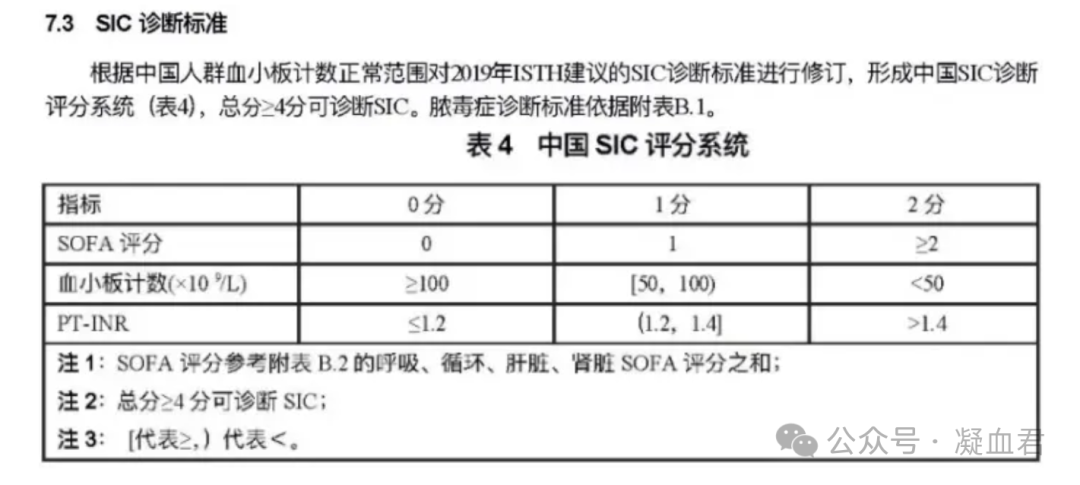
生理性止血是促凝和抗凝途径之间的一种平衡,在脓毒血症中,这种平衡会被破坏,期间凝血酶大量生成,抗凝活性明显受损,纤维蛋白溶解受到抑制,这种情况称为脓毒血症诱导的凝血病(SIC)[1]。SIC是一种常见的并发症,在24%的脓毒症患者和66%的脓毒症休克患者中存在,并且通常与临床预后差和高死亡率相关[2]。SIC由先天免疫系统和凝血系统之间的病理相互作用引发。其特点是全身炎症和凝血激活,导致微血管血栓、器官灌注受损以及随后的器官功能障碍。SIC与DIC存在差别,在DIC 中,存在总体消耗性血管内凝血病,这意味着血小板、纤维蛋白原和凝血因子显著减少,并有血栓和/或出血倾向的临床证据。相比之下,SIC是一种非显性 DIC,也表现为全身性血管内凝血,但没有血小板、纤维蛋白原和凝血因子的总体消耗,并且通常先于 DIC 失代偿性凝血病发生。下图为ISTH overt DIC and SIC评分系统[3]。近期中国医药教育协会血栓与止血危重病专委会在南昌发布的《凝血障碍诊断规范》团体标准如下图,其中血小板计数相比ISTH对SIC的诊断标准有所变更,更改为与DIC诊断标准一致。
在脓毒症中,单核细胞被认为是内源性TF的主要来源, 已证实动物和人类脓毒症患者血浆中TF和含TF微粒水平升高 [4],并认为这是血管内凝血酶生成的驱动因素,证实单核细胞在内毒血症反应中生成血浆TF的首要作用。随后,凝血酶可通过蛋白酶激活受体 (PAR) 与单核细胞相互作用,进一步增强TF的表达,形成白细胞活化、TF表达和凝血酶生成的正反馈回路。通过激活的循环单核细胞增加促凝组织因子(TF)表达、促进凝血酶生成的中性粒细胞胞外陷阱 (NETs) 形成、伴有内皮损伤的明显血管炎症以及受损的抗凝机制是SIC 病理生理学基础(如下图)。脓毒症期间微生物释放PAMP,或受损宿主细胞释放DAMP,这两者都会导致免疫细胞活化和单核细胞、内皮细胞和中性粒细胞的TF表达,随后产生凝血酶,凝血酶是自身增殖的强大正反馈信号从而导致大量凝血酶产生。此外,活化的NETs可作为多聚阴离子表面,进一步生成凝血酶。血小板脱颗粒、白细胞TF表达、NET形成和PLA形成促进(虚线)凝血酶生成,导致纤维蛋白生成和血小板消耗,从而导致微血管血栓形成[1]。
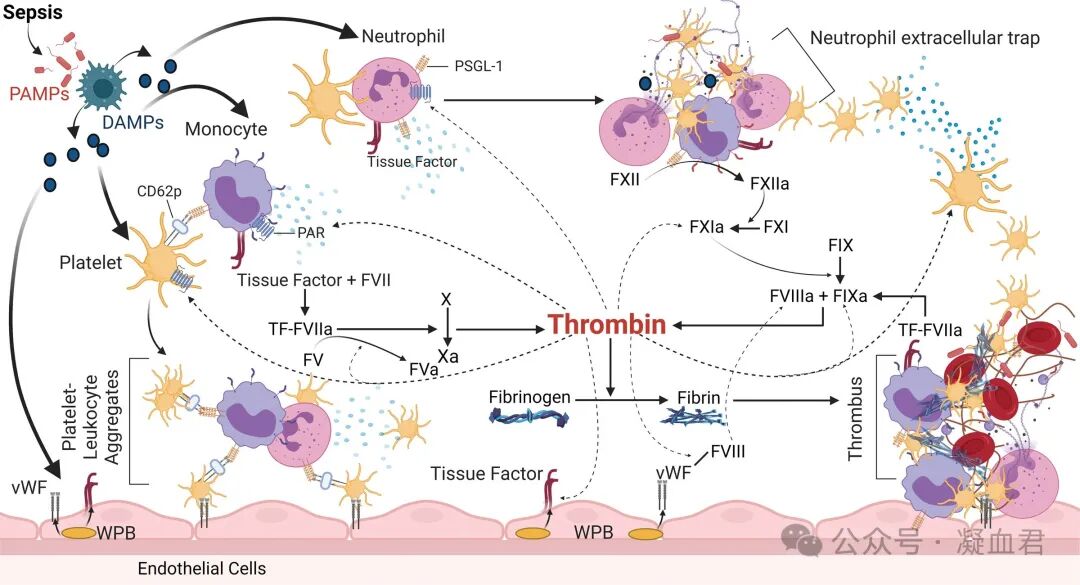
DAMP 表示危险相关分子模式;NET 表示中性粒细胞胞外陷阱;PAMP 表示病原体相关分子模式;PLA 表示血小板-白细胞聚集体;PSGL-1 表示 p-选择 (CD62p) 糖蛋白配体-1;TF,组织因子;vWF,血管性血友病因子;WPB,韦贝尔腭小体。
病原体相关分子模式(pathogen associated Molecular Patterns, PAMPs)在SIC中起关键作用。PAMPs是病原体的糖蛋白、膜组分和核酸的分子片段。这些分子的模式被宿主受体识别,包括toll样受体(TLRs) ,并触发先天免疫系统的细胞和非细胞成分的激活,细菌细胞膜成分是公认的PAMPs,其中一些与促凝活性直接相关。危险相关分子模式 (DAMP) 是宿主细胞在应激条件下释放的内源性生物分子,可触发先天免疫反应。DAMP被公认为脓毒症中免疫失调和促凝信号的介质。它们包括核结合蛋白以及核酸,可通过TLR依赖性或非依赖性途径发出信号。

SIC 是脓毒症的一种并发症,凝血障碍与先天免疫激活有关,并引起器官损伤和高死亡率。虽然免疫介导的凝血酶生成、血小板活化、内皮损伤和抗血栓机制受损发生各自独立,但它们在SIC的发病机制中以协调的方式相互作用,抗凝治疗可能会改善脓毒症患者的预后。
